リンク
組織概要
医理工学グローバルセンターの創設までの経緯
はじめに 「医理工学研究」の黎明期 「医理工学研究」の促進期 部局間連携と大型産学連携へ 医療情報のデジタル化に関する医理工研究 国際連携研究教育局(GI-CoRE)量子医理工学グローバルステーション(GSQ) 「医理工学院」の創設 医理工学研究教育組織の「内在化」 医理工学グローバルセンター 病院の医学物理部 おわりに
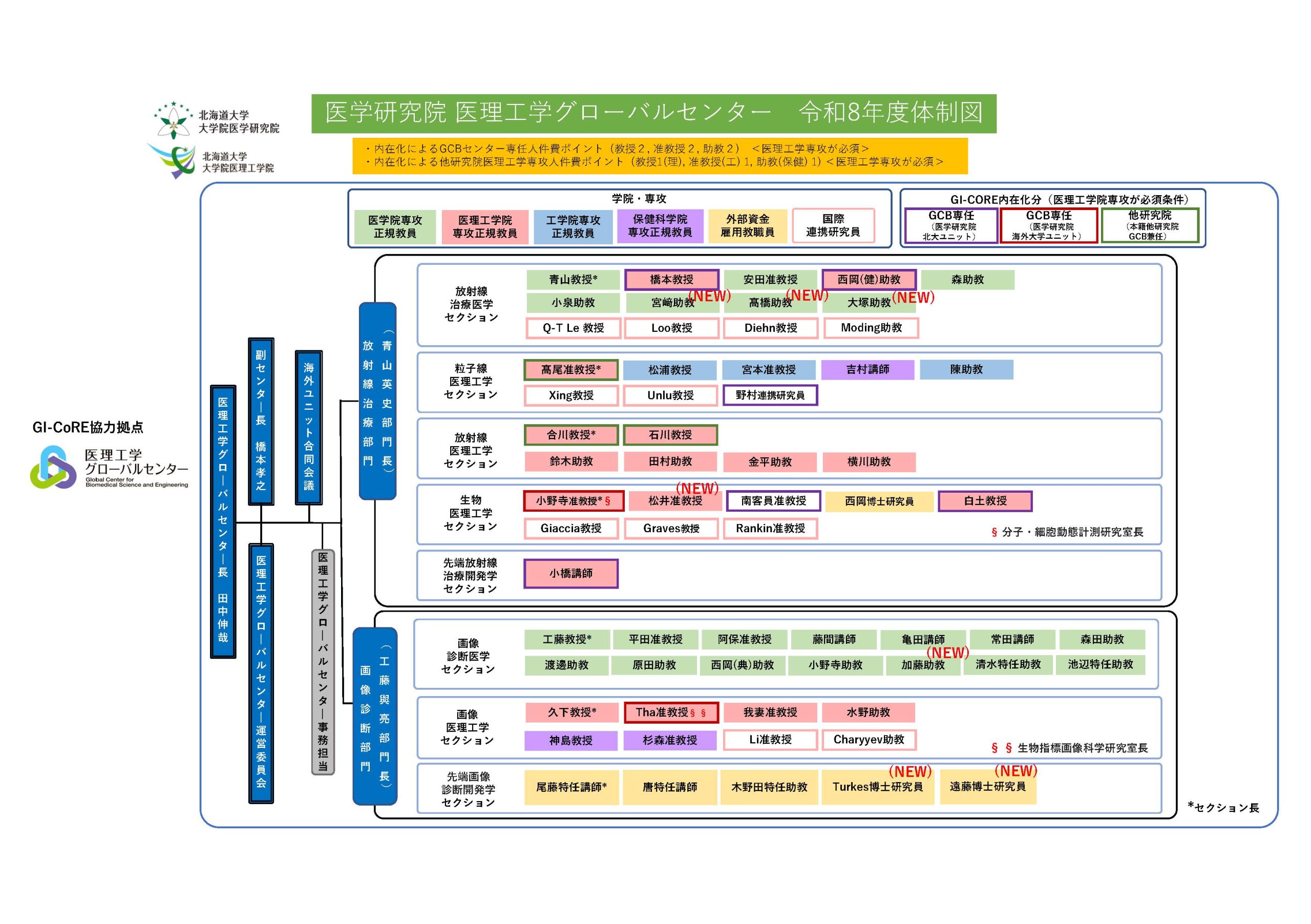
組織体制図
1.はじめに
今から2400年前頃、医学の父といわれているヒポクラテスは、医療における倫理観の大切さと患者の客観的観察に重きをおき、それまでの呪術や迷信から脱却したそうです。一方で、その後の各時代において、個々の医師は倫理観を持っていたにもかかわらず、理工学に関する科学的知識が不足していたために、現在では考えられないような不合理な医療が行われていた例があるのも事実です。
医学の進歩のうち、その約半数は医学には全く関係のない理工系の科学技術の発展に因っていると言われています。中でも、20世紀に花開いた量子論・加速器・電子工学等を医学に応用する分野は、これらがカリキュラムにない医学部医学科の教育内容だけでは理解ができないことが多いのが実態です。さらに、情報科学と分子生物学がそれらに融合した21世紀の今、人体の生理・疾病の病理を解明し、病いに苦しむ人を助けるには、従来の基礎医学・臨床医学の研究者や既存の医療従事者だけではなく、理工系の最先端科学技術を医学に活用できる理工系人材が必須です。
そのような人材の育成を行うことを目的として、2017年4月1日に、北海道大学大学院に、新たに「医理工学院」が発足しました。医理工学は新しい言葉ですが、生命現象の解明、疾病の克服、人類の健康の増進に向けて、理工学の知識や技術を活用して研究する学問です。生命・疾病・人間の健康の本質を科学的に追及し、その研究結果が医療の発展に結びつき、世界の人々が平安な日々を送るために役立つことを目指しています。
さらに、医理工学の国際的な研究と人材育成の場として、2020年4月1日に、北海道大学医学研究院に医理工学グローバルセンターが発足しました。本センターでは、高い倫理観をもって、最先端の理工学を用いて医学的命題を追及し、最先端技術の医療への正しい応用を目指す研究を行い、新しい医療技術や医療機器を開発し、今まで治らなかった疾病を一つでも多く診断し治癒に導くことが期待されます。
ここに至るまでには、黎明期の関係者の先見性、当事者らの寝食を忘れての研究、支援者らの献身的努力の積み重ね、平和な社会情勢などの幸運があったことが、思い返されます。しかし、「不言実行」が美徳とされる我が国では、ともすると、それらの歴史が時間とともに人々の記憶から消失し、組織の源流をたどることが困難となることが多いのも事実です。「医理工学グローバルセンターの創設」に至るまでにどんなことがあったのか、できるだけ客観的な経緯を記載しておきたいと思います。
なお、以下の文中で、敬称は略させて頂きます。
2.「医理工学研究」の黎明期
1895年11月8日に、物理学教授だったレントゲン博士が、大きな誘導コイルからの放電電流を真空管に通し、「蛍光版の前に私が手をかざしてみると、手の中の骨がはっきりと見え、周りの軟部組織はかすかなシルエットとなって、薄く見えた」(Science 3;227-231, 1896)と報告したのが医理工学の始まりと考えます。その後、放射性物質、光電効果、素粒子論、相対性理論、電子計算機など、19世紀までの工学では理解できない新たな学問を、理工学研究者が20世紀に発展させ、それらが医学に応用されてきました。
北海道大学では、戦後、1946年の応用電気研究所を経て、1949(昭和24)年に医学部放射線医学講座ができます。同講座の初代教授若林勝は生理学教室を経て応用電気研究所の出身者、第2代教授入江五朗は北大理学部に入学したあとに医学部入学をした方々で、当初は「医学」講座というよりも、「医理工学」講座と言うべき研究をされていました。1950年代は放射線間接作用の研究、1960年代前半は3次元的に照射部位を把握できる固体線量計の研究等での論文・学会発表が多く、1960年代後半は子宮頸がんを治療するラジウム治療において術者が被曝しないように遠隔操作を取りいれた企業(島津製作所)との産学連携研究(1)、1970年代は大型計算機を用いた患者データベース構築、1980年頃からは放射線治療計画用CT装置の企業(島津製作所)との研究開発などをされています(2)。
1980年代からは、我が国の臨床現場での放射線科医師の需要が一気に高まり、放射線科の医師は画像診断と放射線治療の病院内での業務が日常のほとんどを占め、学会発表も臨床研究が主流となり、かつてのような「医理工学」的な研究をする教員・学生は激減しました。それまで交流のあった理工系教室との連携研究の灯も細くなり、医学部南棟1階西端の教室にあったX線撮影装置・フラスコやガスバーナーなどの実験用具は消え、実験室や写真現像用暗室は文字通り「医師の物置」と化し、そのうち、姿を消しました。放射線科では、海外から輸入した診断・治療装置を用いることが増え、国内の医療機器開発企業との産学連携研究は減りましたが、それに代わって優れた臨床研究が増えました。
1980年代後半、入江は、放射線治療学から医療情報学に研究の主軸を移し、後に述べるように病院全体のCTやMRIの医療画像情報を一元管理し、病院内外に伝送できるようにするPACS(Picture Archiving and Communication System)を企業(NEC)と共同開発し、医療情報学と放射線科学との両者をつなぐ「医理工学」で貢献しました(3)。
3.「医理工学研究」の促進期
1980年以降、放射線科学は一層複雑となり、放射線治療における物理学的な知識の重要性が増しました。欧米では、理工学系のバックグラウンドを持つ修士・博士課程出身の研究者が、病院内で放射線治療の品質管理を担う重要な職種である医学物理士(Medical Physicist)として活躍し、WHOやIAEAでもその職種は必須であると勧告されるようになりましたが、我が国では、医師と優秀な診療放射線技師が、その業務を肩代わりしていました。我が国でも理工学系の研究者の病院業務への参入が放射線科学の発展には欠かせないと考える方が増えましたが、しばらくは、医師や技師が代わりに自分らが手弁当で勉強して「医学物理的」な研究を見様見真似で始めるしかない状況でした。1980年代後半、入江のもと、辻井博彦、溝江純悦、有本卓郎、鎌田正らが、渡辺良晴技師らとともに、治療計画用CT装置を活用して3次元的照射精度を高め、細いX線ビームを用いた肺がんへの3次元大線量寡分割を、おそらく世界で初めて行いました。
1990年代前半、白土博樹がCTや血管造影を基に頭蓋内病変に対して±1mmの精度で手術が可能な「駒井式」脳定位手術用頭蓋固定装置を改良し、脳内深部の腫瘍に体外から正確にX線治療をするための固定装置と計算ソフトを自主開発しました。この計算ソフトは、原理はハーバード大学の論文を参考として、白土がBASICで基盤のプログラムを書き、松沢徹医師らの能力を借りて完成されました。渡辺、藤田勝久技師らとリニアックを定位放射線治療用に改良し、鈴木恵士郎、西岡健、影井兼司らと頭蓋内腫瘍、聴神経鞘腫、脳動静脈奇形等への臨床研究を行いました。その後、「駒井式」脳定位手術リングを開発していた瑞穂医科工業がこれに興味を持ち、MRIも用いることができる脳定位放射線治療用頭部固定装置と計算ソフトを北大と共同開発し、RADFRAMEとして市販しました(4)。青山英史らは、この装置などを用いて、転移性腫瘍への多施設共同臨床研究等を精力的に行い、その成果を世界有数の医学雑誌に発表し、上位1%引用論文を含めて国際的に高い評価を得ました(5)。
1995年頃からは、体内の腫瘍が呼吸などで上下左右に動くような肺癌や肝癌、腸内のガスなどで場所が微妙に変化する前立腺癌などにも体外から正確に照射するための研究を、清水伸一らがCTやMRIの画像解析を用いて行いました(6)。また、白土らは、脳定位照射で実現した精度を体幹部に拡大すべく、1997 – 1998に科研費(B)「動体追跡照射法」にて、三菱電機の研究所にいた国枝達也と共同で基盤研究を行いました。X線透視装置のビデオテープに録画した1-2mmの金マーカーの動きを、当時の理工学では最先端技術であった「リアルタイム動体追跡プログラム」を用いて、パターン認識技術で0.03秒毎に認識できました。金マーカーが計画した3次元座標から±1~2mmの範囲に位置している場合だけ照射する放射線同期照射技術を考案し、国際特許 (三菱電機50%、北海道大学50%)を取得し、1998年に「動体追跡X線治療装置」として実機を開発し(7)、清水、鬼丸力也、喜多村圭らにより多くの論文が発表されました。「動体追跡装置で得られた体内の金マーカーの動きのデータ」は、長い間、世界的にも北大の動体追跡装置でだけ取得可能なデータであったため、ハーバード大学やオランダ国立がんセンター等から研究者が札幌に集結し共同研究を行いました(8, 9,10)。2000年台には動体追跡照射技術に関する論文の引用回数は、上位1%以上となることが頻繁となりました。
1995年に、玉木長良が京都大学から核医学講座教授として赴任し、北海道大学病院にサイクロトロンのポジトロンCT(PET)が導入され、核医学研究を発展させるために、1999年に医学部初めての寄付講座「トレーサー情報解析学講座」が開設され、志賀哲が臨床系、久下裕司が薬剤系、加藤千恵次が計測系を担当し、定量性の高い解析を可能としました。
1996年頃から、西岡が、頭頸部がんの放射線治療の効果予測のための分子生物学的研究を開始しました。西岡は、若くして保健科学研究科教授となり、放射線生物関係の科学研究費を、研究代表者として2014年までに基盤(B)を4回取り続け、分子生物学と放射線治療との融合研究の土台を作りました。
これらの裏話を1つ、ご紹介します。「動体追跡装置で得られた体内の金マーカーの動きのデータ」のもともとのローデータは、患者の体内の動きとは異なる、技師による患者の体動の調整などのアーチファクトが入っており、そのままでは使い物になりません。それらを、体内の動きの貴重なデータと識別するのは、清水ら「医師による、理工学者が解析するために必要なデータ・クリーニング」の地道な作業でした(14)。逆に、理工学者が装置からのノイズを削除して解析してくれた結果を、医師らが学会で発表することも数多くありました。医療情報すべての「データ・クリーニング」は下請け作業であり、決して、派手な注目を浴びることがありませんが、実際には、「医・生物系」と「物理・工学系」がお互いを尊重して、このような裏方の作業ができる体制が、「医理工学」研究の本質でもあります。
4.部局間連携と大型産学連携へ
2004年の春先に、工学部の鬼柳義明教授が医学部放射線科宮坂和男教授を訪ね、粒子線治療施設の北海道大学への導入を目指さないかというご提案をされました。事務局を当時放射線治療のヘッドであった白土が担当し、2004年6月15日(火)に、全くの手弁当で、第一回北海道医工創成プロジェクト発起人準備会が開かれました。場所は、医学部放射線科教室会議室(当時は南棟一階)で、医学部医学科から宮坂、玉木、白土、工学部から澤村貞史、榎戸武揚、只野 茂、鬼柳、医学部保健学科から伊達広行、加藤が参加しました。プロジェクトグループの愛称はPOLARISとし、Particle, Oncology, Light, Atom, Radiation, and Imaging Scienceの略で、粒子線治療だけではなく、腫瘍学、光、原子、放射線、画像科学を包含して、医学、工学、理学を融合した研究を進めることにしました。POLARISとは北極星であり、「さまざまな思惑や流行でうごめく世界の状況に惑わされず、常に進むべき方向を間違わないための指標となるべく、北の星、北海道大学が進めるプロジェクトである意図」をもって付けられました。POLARISの月例会議には、北海道電力や日立や三菱電機をお招きし、粒子線治療施設の導入に係る会議が持たれました。
2005年には、寄付講座「トレーサー情報解析学講座」に続いて、日立による寄付講座「分子イメージング講座」が開設しました。この寄付講座と上記のPOLARISの動きを融合したプロジェクト「分子イメージング研究を軸とした医工系先端的医療の推進に資する部局・分野横断的研究プラットフォームの構築」が、北海道大学本部から戦略的プロジェクト研究として支援を受けることになりました。
2006年には、地域貢献と医学物理士の育成のために設立された北海道大学病院分子追跡放射線医療寄付部門(寄付母体:北海道電力等)が設立されました。すでに医学物理士を取得していた石川正純、同教室にきてから医学物理士を取得した鈴木隆介、宮本直樹、さらにジェラード・ベングア、ケネス・サザーランドらが、病院内での同寄付部門において理工系博士として活動を開始しました。実は2004年に三菱電機がX線治療分野から撤退したことに伴い、同社が保有していた動体追跡照射技術の特許50%の部分を北海道大学に無償で譲渡したいという申し出があり、同知財は北海度大学の100%保有特許になりました。この分子追跡放射線医療寄付部門が、三菱電機から受け継いだ動体追跡技術の灯りをともし続け、そのプログラムを汎用可能な状態にしたことは、のちに、北海道大学の医理工学研究の最大の特徴となり、動体追跡照射技術に関連した大型研究開発に繋がりました。
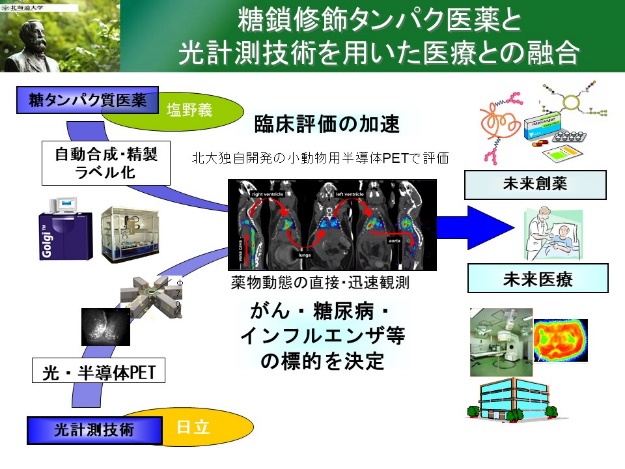
同じ2006年、上記の動きを基に、当時の本間研一研究院長、玉木、白土らは、五十嵐靖之先端生命科学研究院長らと連携し、大型産学連携研究(10年間で約100億円)「未来創薬・医療イノベーション拠点形成事業」(以下、イノベーション)を獲得し、分子イメージングに関する医理工学研究を10年間に渡り、塩野義・日立・三菱重工等と産学連携で行いました。その過程で、北海道大学側では久下、加藤、石川、日立側では、梅垣菊男らが活躍し、半導体PET装置の開発などの成果を挙げました。また、タ・キンキンがMRI画像の画像解析、武島嗣英が放射線治療と免疫治療の融合研究、南ジンミンは放射線分子生物学、小野寺康仁は創薬グループと分子生物学研究を行いました。
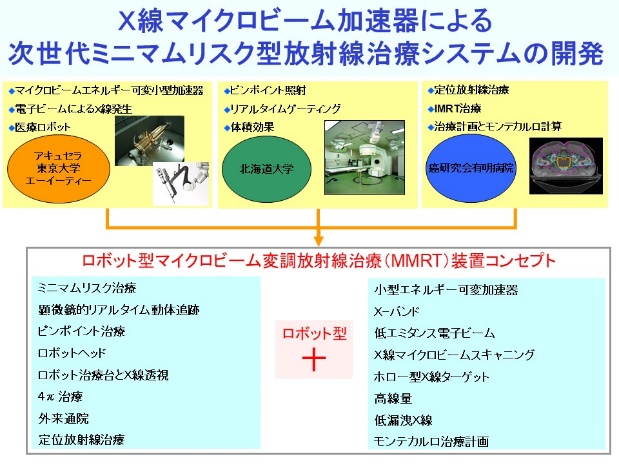
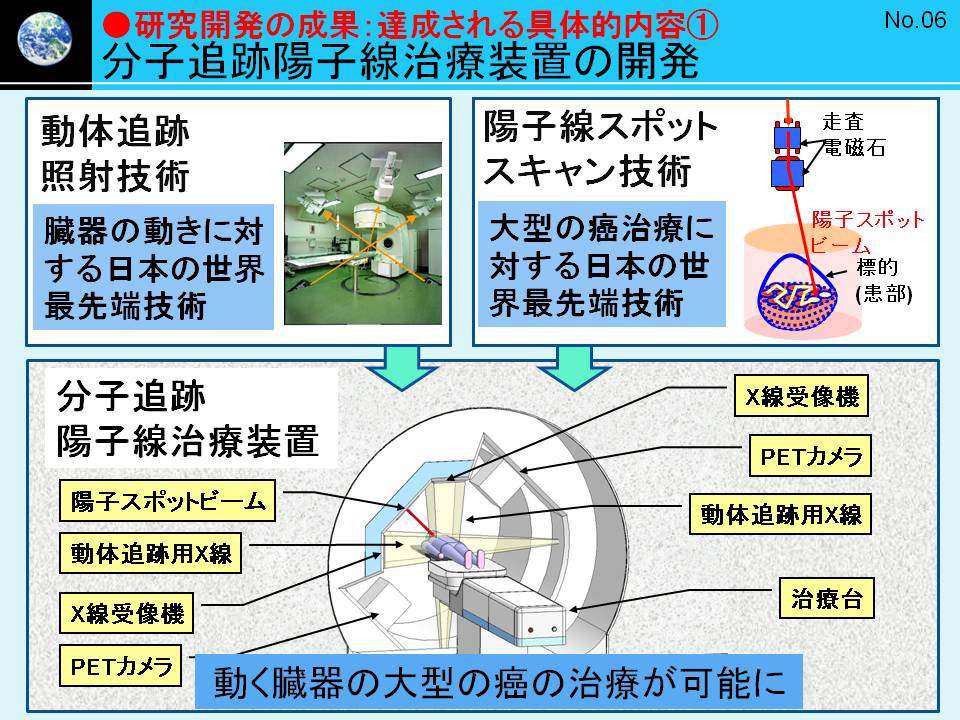
図1.イノベーション拠点形成事業のヒアリングで用いられた資料 図2.NEDOでの小型X線治療装置開発のヒアリングで用いた資料 図3.最先端研究開発支援プログラム(FIRST)のヒアリングで用いた資料 5.医療情報のデジタル化に関する医理工研究
入江は、放射線科研究者としてのほかに、医療情報学研究者としても大きな業績を残しました。1976年に北大病院の電子計算機システム検討委員会の委員長として、1979年に医事システムとして電子計算機を病院に導入しました。また、理工系研究者伊藤佐智子を助教として雇用し、北海道大学の大型計算機を利用し、医療情報の電子化の研究を進めました。ベンチャーであったSORDや大手のNECなどと早くからカルテや医療用画像の電子化に関する研究開発を進め、1988年に北海道大学病院医療情報部の初代部長となり、NECとの共同開発にて、オーダリングシステムとともに当時世界最大級の画像情報システムPACSを全病院規模で運用開始し、世界中から注目を集めました。
1992年に入江が鬼籍に入り、その後、医療情報部長には、検査部教授小林邦彦が2代目、放射線医学分野教授宮坂和男が3代目、医学研究科医療情報学分野教授の櫻井恒太郎が4代目となりました。この間、医療情報部の人材不足もあり、放射線科の寺江聡、工藤興亮、白土らと放射線部の渡辺技師ら、放射線科病棟の看護師らは医療画像、診療録、看護記録、温度板の完全電子化のため、診療録管理ワーキンググループ(WG)・電子カルテWG・フィルムレスWG等で、理工系出身の遠藤晃らと医療情報システムの仕様書作成にかなり多くの時間を費やしました。当時は、正式な共同研究契約を結ぶことなく、導入された医療情報システムの実装協議という形でした。NEC社の「画像情報システム」、「看護支援システム」、「電子温度板」、携帯端末でのベッドサイドでの情報入力システムに関しては、当時の放射線医学講座の教員がかなりのアイデアを出しました。現在のNECの医療情報システムに連結している画像管理理ステムや看護情報形態端末「らくらく看護師さん」や患者の体温が経時的に表示される機能は、本学とNEC社の医理工学的研究成果と言えます。
2004年4月にはWindows Officeが使える「電子コメント」機能をNECと開発し、これを用いてカルテ記載項目の電子化を全科で利用開始し、段階的な完全電子カルテ移行への第一歩を踏み出しました。また、2004年5月には、一部を除いて全病院の医療用画像のフィルムレス運用に成功しました。他にも、多くの診療科の医師が関わっていたと思われ、現在、NECの医療情報システムで、完全な電子化に移行できたこれらの壮大な事業は医療者と医療情報部のみでなく、各関係科とNEC社の医理工学と情報学の理工系研究者の成果と言えます。
これらのソフト関係の開発に関しては、もし、共同研究契約を結んでおけば、もっと大学の研究としての成果としてカウントできていたはずで、今後、医理工学グローバルセンターとしては、ソフト開発を産学連携で行う場合に留意して進められることが期待されます。2008年からはJ-Macという会社と、がん治療の選択を患者視点で行える「がん診断・治療ナビゲーションシステム」のソフト開発をNEDOやAMEDの大型研究費を獲得して行いました(白土、安田耕一等)。これを市販化し、現在一部を特許化しつつありますが、まだまだ、産学連携研究としては細いものです。
以上のように、今後は、医療情報関係の企業との医療現場に直結するソフト開発などの産学連携研究にも期待がかかります。
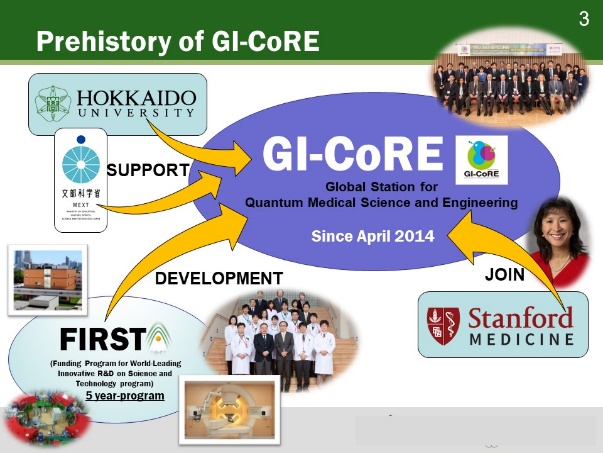
6.国際連携研究教育局(GI-CoRE)量子医理工学グローバルステーション(GSQ)
2010年度以降、分子追跡陽子線治療研究は欧米やアジアから高い注目を浴び、FIRSTに関連した公的資金を相次いで獲得し、国際シンポジウムを毎年開き、研究拠点の様相を帯びてきました。いっぽうで、FIRST終了後の長期的な医理工連携・産学連携研究と人材育成を続けるためはどうすべきか、日立からの出向から工学研究院の正規教授に立場を変えていた梅垣ら理工系教員と頭を悩ませ、大学本部にも相談しておりました。
2012年度に、大学本部から、世界トップレベル研究拠点プログラム(WPI)へ「生命動態追跡医科学拠点」の申請をするように言われました。動体追跡技術・分子イメージング・医療材料・放射線治療学を基盤とした拠点のアイデアを提案し、スタンフォード大学の医学物理学教室からLei Xing教授、放射線生物学教室からAmato Giaccia教授、放射線腫瘍学教室からQuynh-Thu Le教授などがPIとして参加する許諾を得ました。本学内部での厳正な審査ののち、北大としてWPIに申請することになりましたが、北大からは獣医学研究科からも人獣共通感染症に関するWPI申請があり、北大として一本化することはしなかったところ、どちらもWPIは採択には至りませんでした。
翌年、学本部から我々医理工学関係者と獣医学研究科に、本学の機能強化の一環として、海外の一流大学からユニットごと研究者を誘致するアイデアが大提案されました。そして、我々は、陽子線治療センターを基盤として、国際連携研究に関して何かできないかと打診を受けました。その前年のWPIへの申請時に快諾してくれていたスタンフォード大学の研究者らに相談すると、今回も協力してくれることになりました。安田和則理事らとスタンフォード大学に赴き、同大学と本学本部・文部科学省と折衝を繰り返し、「ユニットごと誘致」が次年度からの特別予算(運営費交付金のうち時限付きの予算)枠で認められました。
2014年度からは、文部科学省の特別経費「国立大学の機能強化(組織整備、プロジェクト分)」等を用いて、総長直下の国際連携研究教育局(以下、GI-CoRE)に量子医理工学グローバルステーション(GSQ)を立ち上げ、北大とスタンフォード大学の優秀な教職員を札幌の北大キャンパスに集め、医理工学の国際連携研究と人材育成を行い、さらに発展させることになりました。同時に獣医学研究科にもグローバルステーションができました。いわば、小型版WPIが二つ、北大にできました。
図4.GI-CoRE GSQの立ち上げ時の説明資料 図5.第4回GI-CoRE GSQサマースクールと第7回GI-CoRE GSQシンポジウム 7.「医理工学院」の創設
2013年度に、「ユニットごと誘致」が次年度の特別予算枠として認められた背景には、もうひとつの理由がありました。当時、大学としては、教育改革として、大学院生と教員が同一の組織に所属する「研究科」単位から、大学院生の所属する「学院」と「研究院」とに分離する「学院・研究院」構想を進めようとしておりましたが、医学研究科や歯学研究科にとって学院と研究院に分離するメリットは明らかではなく、反って教育負担が増えるのではないかと、だれも興味を示しておりませんでした。そんな中、国際連携教育を実現するために、上記の「海外からのユニット毎の誘致」に「学院・研究院への組織改変」を抱き合わせた案を考えてほしいという示唆が、大学本部からありました。
たまたま、医学研究科では、文部科学省「がんプロフェッショナル養成プログラム」等の支援を受け、病院の分子追跡放射線医療寄附研究部門、FIRSTなどで北大に集結していた医理工学研究者らとともに「医学物理士プログラム」を医学研究科、工学院、理学院の修士・博士それぞれの大学院課程において開講しておりました。よって、「医学物理士プログラム」関係者は、医学研究科が学院・研究院に改組すれば、医学研究科、工学院、理学院が別々にプログラムを行う必要がなくなるため、ありがたいと思っておりました。さらに、大学本部としては、「ユニット毎の誘致」に学院・研究院の改組を伴う場合には、文科省からの特別経費に加えて、総長裁量経費を用いて任期付き正規教員(2.5ポイント分)を雇用できるようにするとのことでした。この本部からのご提案は、外部資金で多くの研究者を雇用していたFIRST関係者にとっては、渡りに船でありました。
白土らは、生命科学院や化学院の設置時の資料を集め、学院・研究院の仕組みを学び、「医学院」とは別に「医理工学院」を設置するという着想に思い至りました。「医理工学院」専任教員として、イノベーションやFIRSTやGI-CoREの任期付特任教員とスタンフォード大学のvisiting scientist教員を充てることで、医学研究科の既存の人件費ポイントはいっさい使うことなしに、本部のいう国際連携教育が可能となることに気づきました。また、「医理工学院」の予定教員は学部教育でも活躍でき、北海道大学病院にて陽子線治療や高精度放射線治療に携わる医師や医学物理士でもあるため、医学部教育や大学病院の経営にもプラスになることから、医学部・病院の負担を減らす効果が大きいこと、また他の医学研究科の教員が他学院を担当できるメリットがあることも、関係者にご説明しました。一方で、大学本部は医学研究科長に対し、医学研究科博士課程は定員100名のところ恒常的に90%未満の充足率で、少し大学院学生定員を減らしてでも充足率を100%にしないと、教員数を減らされるリスクがあると常々指摘しておりました。よって、「医学研究科を医学院・医理工学院・医学研究院に改組」して医学研究科の大学院学生定員の一部を医理工学院に振り替えることは、医学院の充足率を100%に改善でき、さらに医学研究院全体の教員数は医理工学院専攻教員の教員数分増えることになるため、医学研究院にとってそのメリットが明らかでした。最終的に、2016年8月25日開催の医学研究科教授会にて「医学研究科から医学院・医理工学院・医学研究院」への改組が認められました。ちなみに、その後、医学院の博士課程の充足率は改善し、毎年、目標を達成しています。
図6.医理工学院の開設時のパンフレット 8.医理工学研究教育組織の「内在化」
2019年度からは、医理工学の研究と医理工学院での人材育成の成果と将来性を評価され、医理工学院専任教員の人件費と研究費に関して文部科学省から予算の「内在化」(運営費交付金のうちの時限付き予算から一般予算への変更)が認められました。
図7.内在化に向けて総長ヒアリングで利用した資料 図8.総長ヒアリングで使われた創設時のGCBのイメージ図
医学研究院では、放射線医理工学教室に、教授1名、准教授1名、助教1名の正規ポストが配置され、医学院担当の他教室と同等な基盤教室ができました。初代の教授と准教授と助教としては、それぞれ清水伸一と橋本孝之と西岡健太郎が赴任しました。
医学研究院連携研究センター陽子線治療医学教室の教授用1.0ポイントは、白土博樹が退職する2022年度以降は、医学研究院全体のポイントとすることとし、医学研究院に対してプラスとなる措置であることを明確にしました。
GI-CoRE GSQを内在化した後継組織として、次に述べる医理工学グローバルセンター(GCB) を医学研究院内に設置し、医理工学院専攻の教授または准教授1名、准教授1名、助教1名のポストを配置することとなりました。初代は、准教授キンキンタ、講師南ジンミン、助教ケニス・サザーランドでスタートしました。
その他の部局には、医理工学院を担当することを条件に、理学研究院には医理工学院医療基礎物理学分野に教授1名、工学研究院には医理工学院放射線医学物理学分野に准教授1名、保健科学研究院では教授あるいは准教授計2名が医理工学院医学物理学分野および医用画像解析学分野を担当し、同2名の保健学科の教育負担の軽減のために助教1名のポストを貸与することを、医理工学院長と事務が立ち会いのもと、医学研究院長と各研究院長の間で覚書を交わしました。
工学研究院からは、松浦妙子、続いて宮本直樹、続いて高尾聖心が同ポストを担当しました。
理学研究院からは、それまで総長裁量枠であった合川正幸を2021年度からは内在化された人件費ポイントを活用した正規教員として迎えました。
保健科学研究院からは、加藤千恵次、石川正純が医理工学院を担当し助教1名が雇用されました。
その他、歯学研究科はこれを契機に歯学院・歯学研究院に改組し、そのうち東野史裕は医理工学院を担当することとなり、アイソトープセンターからは、医学院から医理工学院に専攻を変更した久下裕司教授のもと、安井博宣続いて水野雄貴らを正式に迎えました。
この中の多くの方は、長年、不安定な特任教員として、北大での医理工学研究開発において、活躍してきた方々でした。研究開発だけであれば、研究費が切れた瞬間に教員が北大を離れ、研究自体が忘れ去られることも多いです。文部科学省や北大本部や医学研究院の皆様のご理解が得られ、「医理工学院」が創設されたのは、「医理工学」の人材育成のために重要なステップでした。現在、医理工学院全体では、医学物理研究者、放射線生物学者、機械学習の研究者などが「医理工学」の人材育成をしております。繰り返しになりますが、世の中に役に立つ研究を時代に残すためには、地味な「裏方仕事」が鍵を握っています。上記の「内在化」された教員ポストを活用し、学院の専任教員は裏方作業をしっかり行い、全体として、「医理工学」が発展していくことが期待されます。
9.医理工学グローバルセンター
2019年度から、上記の医理工学研究教育組織の医学研究院への「内在化」に伴い、GI-CoRE GSQスタンフォード大ユニットとして育んできた体制を維持し、医理工学院にて英語だけで卒用できるコースを維持し、毎年のサマーインスティテュートにて、医理工学に関する国際連携教育を行うために、医学研究院に医理工学グローバルセンター(GCB)が設置されました。同センターの教授または准教授1名、准教授1名、助教1名は、他の医理工学院専任教員とともにGCBでの国際連携研究の継続・発展をしていくことが使命です。
また、GCBの事務職員として、GSQと同様に、英語に堪能な特定専門職員1名、事務補佐員2名が研究者とは別に予算化されました。
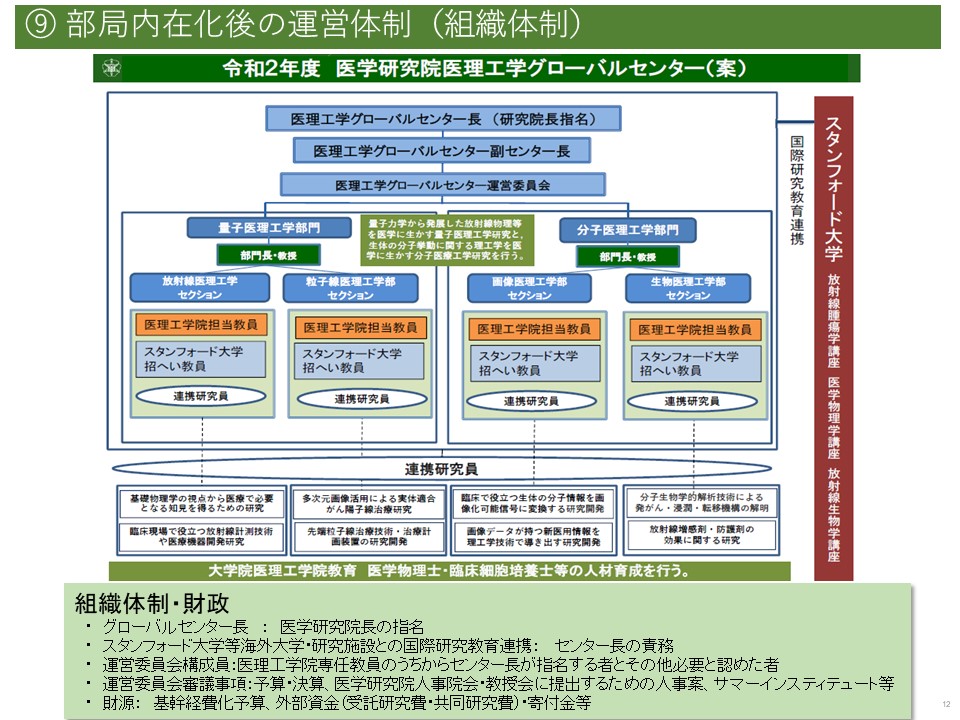
GI-CoRE GSQでは、北海道大学ユニットとスタンフォード大学ユニットの二つに分けられていましたが、GCBではそれらを医理工学院の分野に対応する組織に改組されました。すなわち、センターは、量子医理工学部門と分子医理工学部門の二つからなり、前者には放射線医理工学セクションと粒子線医理工学セクション、後者には画像医理工学セクションと生物医理工学セクションを置き、それぞれのセクションに、北海道大学ユニットとスタンフォード大学ユニットの教職員が混合して配置されることになりました。
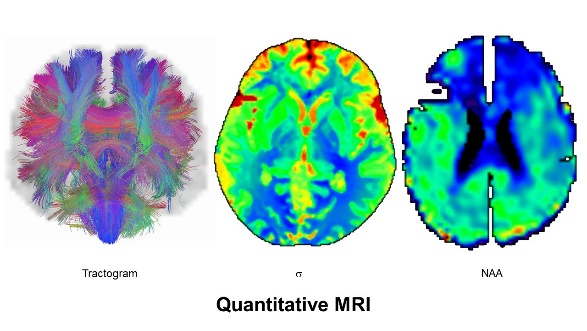
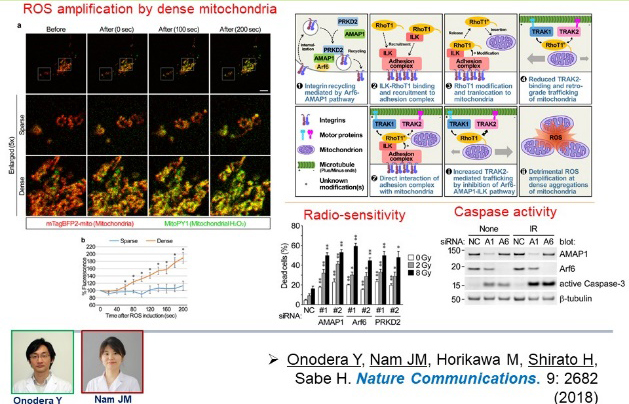
図9.GCBのMRI医用画像研究や遺伝子工学を用いた分子イメージング研究 10.病院の医学物理部
上述したように1980年代から、欧米の大学病院では、放射線理工学を正確に理解している理工系博士の教職員である医学物理士や修士を出られた線量測定士が数多く働いています。各施設毎に医学物理士や線量測定士が、小規模施設で数名、大規模施設では数十名いるのが普通ですが、我が国では、2000年代前半まで北大病院も築地の国立がん研究センターでも0~1人でした。
北海道大学では、上記のように、病院内に分子追跡放射線医療寄付研究部門が設置され、さらに「がんプロフェッショナル養成プログラム」による医学物理士の養成が進み、鈴木隆介が中心となり、放射線治療品質管理委員会の開催を定期的に行い、さらに強度変調放射線治療(IMRT)の品質管理体制を構築していきました。その後、NEDOやAMEDなどの外部資金でも医学物理士が雇用されるようになり、病院で需要が急激に高まったIMRTの治療計画を医学物理士やそれを目指す若手研究者らが研修を兼ねて対応してきました。さらに、FIRSTによる陽子線治療が開始されてからは、それまでの医学物理士の病院経営への貢献も評価され、詳細な収支計画のもと、医学物理士枠として4名が助教として正式に雇用されました。さらに診療放射線技師が線量測定士として2名、陽子線照射担当として2名が正式に雇用されました。
2019年度からは、医学物理部が正式に発足しました。医学物理部には、医理工学院の創設にも大きく貢献した工学研究院の工学院専攻教員であった梅垣菊男、松浦妙子、宮本直樹らとも連携して、大学院生の教育にも携わっています。医理工学院には、医学物理士コースが開設され、病院医学物理部での実習が博士課程のカリキュラム内に入っております。
今後、医学物理士の国家資格化などキャリアパスが明確になることが望まれますが、国家資格化のためには、国内に放射線技師や臨床検査技師や臨床工学技士とは異なる教育課程が存在することが重要であります。大学に医理工学院が存在し、その卒業後の出口として、医学物理部が大学病院に存在することは、車の両輪として、他大学の模範となりえる人材育成基盤であり、医学物理士の国家資格化のためにも意義深い形であると思います。
11.おわりに
ドルトンやアボガドロの原子・分子説からまだ200年、ハイゼンベルグやシュレデインガーらの量子力学からまだ100年、シュレデインガーの「生命とは何か?」からはわずか70年しか経っていません。長い医学の歴史を振り返り、現代の量子理工学が複雑で難解であることを思うとき、今は想像もつかない医療技術・装置を、今後、医理工学院の卒業生が発明し開発する可能性は極めて大きいと思います。
医師だけでは対応できない今後の医療を考えますと、医学研究院医理工学グローバルセンターの意義が今度益々大きくなっていくことは疑いようがありません。
今後とも、皆さまのご助言、ご支援、ご鞭撻のほど、なにとぞよろしくお願い申し上げます (2021年3月.文責 白土博樹)。
主要な研究業績
Wakabayashi M, Irie G, Sugawara T, Mitsuhashi H, Yamaguchi N. [New remote afterloading system]. Rinsho Hoshasen. 1966 Aug;11(8):678-84. Japanese. PMID: 5182450.
Tsujii H, Kamada T, Matsuoka Y, Takamura A, Akazawa T, Irie G. The value of treatment planning using CT and an immobilizing shell in radiotherapy for paranasal sinus carcinomas. Int J Radiat Oncol Biol Phys. 1989 Jan;16(1):243-9. doi: 10.1016/0360-3016(89)90037-0. PMID: 2912946.
Irie G, Miyasaka K. HU-PACS. 10 months experience. Comput Methods Programs Biomed. 1991 Oct-Nov;36(2-3):71-5. doi: 10.1016/0169-2607(91)90049-y. PMID: 1786690.
Shirato H, Suzuki K, Nishioka T, Kamada T, Kagei K, Kitahara T, Morisawa H, Tsujii H. Precise positioning of intracranial small tumors to the linear accelerator's isocenter, using a stereotactic radiotherapy computed tomography system (SRT-CT). Radiother Oncol. 1994 Aug;32(2):180-3. doi: 10.1016/0167-8140(94)90105-8. PMID: 7972912.
Aoyama H, Shirato H, Tago M, Nakagawa K, Toyoda T, Hatano K, Kenjyo M, Oya N, Hirota S, Shioura H, Kunieda E, Inomata T, Hayakawa K, Katoh N, Kobashi G. Stereotactic radiosurgery plus whole-brain radiation therapy vs stereotactic radiosurgery alone for treatment of brain metastases: a randomized controlled trial. JAMA. 2006 Jun 7;295(21):2483-91.
Shimizu S, Shirato H, Kagei K, Nishioka T, Bo X, Dosaka-Akita H, Hashimoto S, Aoyama H, Tsuchiya K, Miyasaka K. Impact of respiratory movement on the computed tomographic images of small lung tumors in three-dimensional (3D) radiotherapy. Int J Radiat Oncol Biol Phys. 2000 Mar 15;46(5):1127-33. doi: 10.1016/s0360-3016(99)00352-1. PMID: 10725622.
Shirato H, Shimizu S, Shimizu T, Nishioka T, Miyasaka K. Real-time tumour-tracking radiotherapy. Lancet. 1999 Apr 17;353(9161):1331-2. doi:10.1016/S0140-6736(99)00700-X. PMID: 10218540.
Seppenwoolde Y, Shirato H, Kitamura K, Shimizu S, van Herk M, Lebesque JV, Miyasaka K. Precise and real-time measurement of 3D tumor motion in lung due to breathing and heartbeat, measured during radiotherapy. Int J Radiat Oncol Biol Phys. 2002 Jul 15;53(4):822-34. doi: 10.1016/s0360-3016(02)02803-1. PMID: 12095547.
Berbeco RI, Nishioka S, Shirato H, Chen GT, Jiang SB. Residual motion of lung tumours in gated radiotherapy with external respiratory surrogates. Phys Med Biol. 2005 Aug 21;50(16):3655-67. doi: 10.1088/0031-9155/50/16/001. Epub 2005 Jul 28. PMID: 16077219.
Takao S, Miyamoto N, Matsuura T, Onimaru R, Katoh N, Inoue T, Sutherland KL, Suzuki R, Shirato H, Shimizu S. Intrafractional Baseline Shift or Drift of Lung Tumor Motion During Gated Radiation Therapy With a Real-Time Tumor-Tracking System. Int J Radiat Oncol Biol Phys. 2016 Jan 1;94(1):172-180. doi: 10.1016/j.ijrobp.2015.09.024. Epub 2015 Sep 25. PMID: 26700711
Matsuura T, Miyamoto N, Shimizu S, Fujii Y, Umezawa M, Takao S, Nihongi H, Toramatsu C, Sutherland K, Suzuki R, Ishikawa M, Kinoshita R, Maeda K, Umegaki K, Shirato H. Integration of a real-time tumor monitoring system into gated proton spot-scanning beam therapy: an initial phantom study using patient tumor trajectory data. Med Phys. 2013 Jul;40(7):071729. doi: 10.1118/1.4810966. PMID: 23822433.
Shimizu S, Miyamoto N, Matsuura T, Fujii Y, Umezawa M, Umegaki K, Hiramoto K, Shirato H. A proton beam therapy system dedicated to spot-scanning increases accuracy with moving tumors by real-time imaging and gating and reduces equipment size. PLoS One. 2014 Apr 18;9(4):e94971. doi:10.1371/journal.pone.0094971. PMID: 24747601; PMCID: PMC3991640.
Yamada T, Miyamoto N, Matsuura T, Takao S, Fujii Y, Matsuzaki Y, Koyano H, Umezawa M, Nihongi H, Shimizu S, Shirato H, Umegaki K. Optimization and evaluation of multiple gating beam delivery in a synchrotron-based proton beam scanning system using a real-time imaging technique. Phys Med. 2016 Jul;32(7):932-7. doi: 10.1016/j.ejmp.2016.06.002. Epub 2016 Jun 10. PMID:27296793.
Shimizu S, Matsuura T, Umezawa M, Hiramoto K, Miyamoto N, Umegaki K, Shirato H. Preliminary analysis for integration of spot-scanning proton beam therapy and real-time imaging and gating. Phys Med. 2014 Jul;30(5):555-8
EC TR 62926:2019. Medical electrical system – Guidelines for safe integration and operation of adaptive external-beam radiotherapy systems for real-time adaptive radiotherapy. https://webstore.iec.ch/publication/34482
Hashimoto T, Shimizu S, Takao S, Terasaka S, Iguchi A, Kobayashi H, Mori T, Yoshimura T, Matsuo Y, Tamura M, Matsuura T, Ito YM, Onimaru R, Shirato H. Clinical experience of craniospinal intensity-modulated spot-scanning proton therapy using large fields for central nervous system medulloblastomas and germ cell tumors in children, adolescents, and young adults. J Radiat Res. 2019 Jul 1;60(4):527-537.
Nishioka K, Prayongrat A, Ono K, Onodera S, Hashimoto T, Katoh N, Inoue T, Kinoshita R, Yasuda K, Mori T, Onimaru R, Shirato H, Shimizu S. Prospective study to evaluate the safety of the world-first spot-scanning dedicated, small 360-degree gantry, synchrotron-based proton beam therapy system. J Radiat Res. 2018 Mar 1;59(suppl_1):i63-i71.
Copyright © Global Center for Biomedical Science and Engineering, Faculty for Medicine, Hokkaido University. All rights reserved.